Врачи нашей онкологической клиники провели успешное лечение новейшим препаратом Халавен (эрибулин) пациентке 55 лет с распространенным раком левой молочной железы 4й степени.
В январе 2015 года, после проведения 3 линий химиотерапии, пациентка отметила значительное ухудшение общего состояния, потерю веса на 20 кг, после чего обратилась к нам в клинику за помощью. При осмотре онколог обнаружил инфильтрацию и язвенные изменения кожи в области левой молочной железы, увеличение надключичных и шейных лимфоузлов. Консилиум врачей клиники «De Vita» принял решение провести два курса противоопухолевого лечения препаратом Халавен (эрибулин) с дальнейшей оценкой эффекта. По окончании двух курсов лечения достигнут поразительный эффект в виде уменьшения инфильтрации, отсутствия язвенных изменений и уменьшения лимфатических узлов на 70% от исходного состояния. На фоне такой выраженной положительной динамики решено продолжить лечение.
Таким образом, хотим подчеркнуть, что внедрение в клиническую практику принципиально новых оригинальных препаратов в сочетании с высоким уровнем профессионализма врачей, несомненно, дает успешные результаты и позволяет значительно продлить жизнь пациенту и улучшить ее качество.
Халавен (halaven) – препарат из группы принципиально новых противоопухолевых средств, используемый для терапии рака молочной железы. Его активным веществом является эрибулин, препятствующий синтезу и росту опухолевых клеток. Проведенные масштабные клинические исследования убедительно показали эффективность Халавена на поздних стадиях рака молочной железы: его применение позволило существенно повысить выживаемость пациентов и улучшить качество их жизни. По результатам исследований было установлено, что эффективность Халавена превышает эффективность других цитостатических средств почти на 20%.

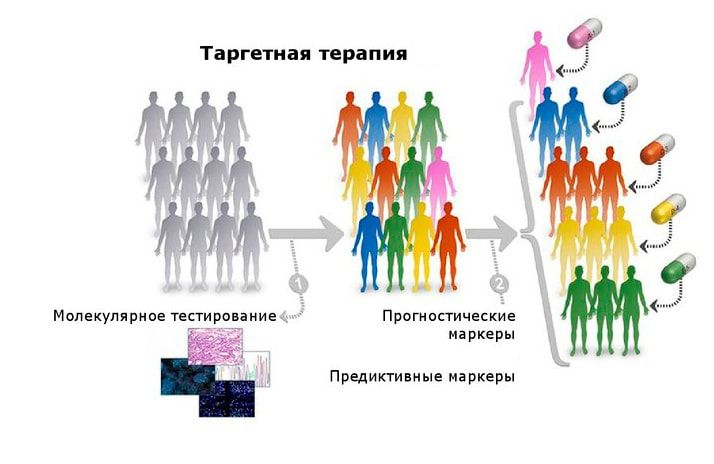
Таргетная терапия в онкологии
Таргетная терапия - что это?
Таргетная терапия в онкологии - это фундаментальное достижение последнего десятилетия, инновационная технология лечения опухолей различных локализаций. Как и химиотерапия, таргетная терапия в онкологии - это системное лекарственное лечение, но она существенно отличается по механизму действия.Принцип таргетной терапии - прицельное, избирательное воздействие на опухолевую клетку. Любой таргетный препарат разрабатывается под конкретную мутацию в определенном гене, поэтому до назначения таргетной терапии обязательно проводят генетическое исследование материала, который был взят на биопсию.
Таргетные препараты блокируют клеточные сигналы к размножению только опухолевых клеток, что останавливает рост опухоли, запуская «запрограммированную смерть клетки» (апоптоз). В то время как химиотерапия останавливает деление всех клеток путем блокировки процессов жизнедеятельности и опухолевых, и здоровых клеток организма.
Наша клиника специализируется на диагностике и лечении редких опухолей с драйверными мутациями в генах EGFR, ALK, ROS1, PIk3CA, BRAF, MET, RET, KRAS, NRAS, NTRK, BRCA1-2.
Целесообразность и подбор таргетных препаратов определяется онкологом-химиотерапевтом на первичной консультации на основании данных иммуногистохимического и молекулярно-генетического исследований.
Таргетные препараты имеют меньшую токсичность на организм и, соответственно, лучшую переносимость, чем химиопрепараты. Большим плюсом таргетной терапии является значительное увеличение эффективности противоопухолевого лечения, продолжительности и качества жизни пациента - это месяцы и годы жизни.
Преимущества таргетной терапии
Таргетные препараты в онкологии обладают существенными преимуществами:- Таргетные препараты действуют прицельно, на конкретные "мишени", и поэтому их эффективность предельно высока. Таргетная терапия демонстрирует впечатляющие результаты при злокачественных опухолях, обладающих определенными молекулярно-генетическими свойствами.
При правильно подобранном таргетном препарате пациент с последней стадией рака легкого может жить 3-4 года и более, хотя до таргетной терапии продолжительность жизни пациентов с таким диагнозом, к сожалению, не превышала 6-8 месяцев. - Таргетные препараты обладают меньшей токсичностью и меньшими побочными эффектами, чем химиотерапия, поэтому они хорошо переносятся. Это особенно актуально для пожилых пациентов и тех, кто находится в тяжелом состоянии.
- Таргетная терапия может сочетаться с другими видами противоопухолевого лечения - например, с химиотерапией или лучевой терапией.
Это сочетание не приводит к увеличению побочных эффектов, но значительно повышает эффективность лечения онкологических заболеваний. - Некоторые таргетные препараты в онкологии производятся в таблетированной форме, поэтому их прием может осуществляться дома, в то время как инфузии химиопрепаратов выполняются в стационаре. Многие пациенты на фоне приема таргетных препаратов сохраняют привычную высокую активность и продолжают работать.
- Таргетная терапия может быть высокоэффективна при опухолях, резистентных к химиотерапии, а значит - продлить жизнь пациента на месяцы, а иногда годы.
Как действуют таргетные препараты в онкологии?
В зависимости от точки приложения, мишенями для биологически-направленных препаратов в онкологии являются:
- Рецепторы к эпидермальным факторам роста (EGFR) и факторам роста сосудов (VEGF).
- Белки, осуществляющие проведение митогенных сигналов от рецепторных молекул. Таргетные препараты этого класса блокируют действие конкретного белка, который является причиной трансформации клеток.
- Молекулы, контролирующие запуск и течение программированной смерти клеток.
- Гены,отвечающие за рост и деление опухолевых клеток.
Таргетная терапия - когда применяется?
- Рак молочной железы - Трастузумаб (Герцептин), Пертузумаб (Перьета), Трастузумаб Эмтанзин (Кадсила), Трастузумаб Дерукстекан (Энхерту), Рибоциклиб (Кискали, Рисарг), Палбоциклиб (Ибранса), Абемациклиб (Верзенио);
- Рак легкого - Бевацизумаб (Авастин), Осимертиниб (Тагриссо), Эрлотиниб (Тарцева), Гефитиниб (Иресса), Афатиниб (Гиотриф), Бригатиниб (Алунбриг), Алектиниб (Алеценса), Кризотиниб (Ксалкори), Церитиниб (Зикадиа);
- Рак кишечника - Бевацизумаб (Авастин), Цетуксимаб (Эрбитукс), Панитумумаб (Вектибикс), Регорафениб (Стиварга);
- Меланома - Вемурафениб (Зелбораф), Дабрафениб (Тафинлар), Траметиниб (Мекинист);
- Рак желудка - Трастузумаб (Герцептин), Трастузумаб Дерукстекан (Энхерту), Рамуцирумаб (Цирамза);
- Опухоли головы и шеи - Цетуксимаб (Эрбитукс);
- Рак яичников - Олапариб (Линпарза);
- Нейроэндокринные опухоли - Сунитиниб (Сутент), Эверолимус (Афинитор), Бевацизумаб (Авастин);
- Глиобластома - Бевацизумаб (Авастин);
- Рак почки - Сунитиниб (Сутент), Сорафениб (Нексавар), Эверолимус (Афинитор).
За последние 10 лет в онкологии произошли значительные изменения – лекарственное лечение вышло на качественно новый уровень. Разработаны и внедрены в клиническую практику инновационные препараты, которые позволяют нам уверенно говорить о том, что рак сегодня – это не приговор, это диагноз.
Уварова Светлана Николаевна

Истории лечения наших пациентов таргетными препаратами:
Женщине 60 лет в 2010 году был установлен онкологический диагноз - рак прямой кишки. В одном из стационаров Санкт-Петербурга была выполнена радикальная операция, однако послеоперационная химиотерапия не проводилась. Спустя 12 месяцев, в 2011 году у пациентки появились метастазы в легких, и она обратилась за помощью в нашу клинику. Онколог-химиотерапевт назначил 8 циклов химиотерапии, после проведения которых был зафиксирован частичный регресс опухолевых очагов в легких, однако появились единичные метастазы в печени, что потребовало продолжить химиотерапию по новой схеме, и после еще 8 циклов в 2012 году был достигнут полный регресс опухоли. В течение полутора лет эффект проведенного лечения сохранялся, и пациентка оставалась под динамическим наблюдением лечащего врача-химиотерапевта нашей клиники.
Затем контрольное обследование вновь продемонстрировало прогрессирование болезни, и консилиумом докторов нашей клиники было назначено и проведено еще 8 циклов химиотерапии по прежней схеме, приведшие к стабилизации до конца 2014 г.
Через полгода результаты компьютерной томографии грудной клетки показали прежнее состояние очагов в легких, и для усиления эффекта лечения онкологи нашей клиники подобрали пациентке схему лечения, сочетающую таблетированный химиопрепарат и таргетный препарат – лекарство, нарушающее рост сосудов в опухоли. Подобранная терапия проводилась в течение года, переносилась пациенткой с минимальными побочными эффектами, и позволяла сохранять контроль над опухолью, прекрасное общее состояние и вести активную жизнь.
С конца 2015 года пациентка переведена на динамическое наблюдение с регулярным обследованием, чувствует себя прекрасно. По данным компьютерной томографии от февраля 2016 года сохраняется стабилизация опухолевого процесса. Нельзя не отметить, что на протяжении всего проводимого в эти годы лечения, благодаря использованию оригинальных качественных препаратов и правильно подобранной сопроводительной терапии, удавалось избегать значимых побочных эффектов и осложнений, поэтому качество жизни нашей пациентки было неизменно хорошим, она сохраняла привычный активный образ жизни.
В октябре 2014 года пациенту 42 лет с диагнозом «Глиобластома» была проведена обширная операция по удалению опухоли. Затем врач-онколог назначил курс таблетированной химиотерапии, которую пациент тяжело переносил из-за побочных эффектов и падения показателей гемоглобина.
После лечения пациент находился в ремиссии около полугода. В конце мая 2015 года пациента появились жалобы на нарушения речи, моторики рук, нарушения походки. данные обследований показали прогрессирование опухолевого процесса и продолженный рост очагов в головном мозге.
Пациент обратился за помощью в государственное специализированное учреждение, где ему было отказано по причине того, что возможности противоопухолевого лечения исчерпаны полностью. Все, что ему предложили, - симптоматическую терапию.
Не теряя надежду, родственники пациента обратились в наш центр за консультацией онколога-химиотерапевта. Лично главным врачом центра Уваровой С.Н. была подобрана индивидуальная схема химиотерапии согласно международным стандартам и с применением новейшего таргетного препарата.
После 4 успешно проведенных курсов химиотерапии результаты обследования показали ответ на проводимое лечение - значительное уменьшение опухолевых очагов в головном мозге. У пациента пропали жалобы на шаткость походки, после этого консилиумом докторов нашей клиники было принято решение о продолжении химиотерапии до 8 курсов с коррекцией сопроводительной терапии.
После 8 курсов мы добились регресса опухолевого процесса, пациент сохраняет свой привычный образ жизни и продолжает наблюдаться главным врачом нашего центра.
За годы работы в нашем центре накопился огромный опыт лечения пациентов с опухолями головы и шеи. При лечении опухолей головы и шеи мы используем самые передовые методики и препараты, зачастую недоступные при лечении в государственных учреждениях.
В ноябре 2015 года к нам обратился пациент К. с диагнозом «рак правой небной миндалины» с метастазами в легкие. После осмотра и консультации онколога, консилиум врачей нашего центра назначил пациенту таргетную терапию, рекомендованную NCCN (Национальная всеобщая онкологическая сеть США) и показавшая наилучшие результаты от лечения. В нашей клинике пациенту было проведено 6ть курсов таргетной терапии препаратом Цетуксимаб (торговое название Эрбитукс). Уже после 2х курсов пациент ощутил улучшение самочувствия – значительное уменьшение болевого синдрома, заживление раневого распада.
По результатам рентгенологических методов исследования, после шести проведенных курсов таргетной терапии, был отмечен регресс метастазов в легких и существенное уменьшение основной опухоли. После достигнутых результатов, мы направили пациента на лучевую терапию. В настоящее время, пациент К. находится в стойкой ремиссии, продолжает вести привычный образ жизни. После завершения лечения лечащий врач-химиотерапевт нашего центра продолжает оставаться на связи с пациентом и оперативно отвечает на любые возникающие вопросы. Пациент находится на динамическом наблюдении и приходит в нашу клинику на консультативные приемы с результатами плановых обследований один раз в три месяца.
Женщина 47 лет с установленным диагнозом "рак молочной железы IIIB стадии" обратилась в нашу онкологическую клинику для решения вопроса о назначении терапии по поводу заболевания.
Учитывая распространенный опухолевый процесс, молодой возраст пациентки, ее менструальный статус и высокоагрессивный гистологический вариант опухоли (HER2+), консилиум онкологов нашей клиники выбрал программу NCCN Guidelines version 3.2017 с целью достижения максимального терапевтического эффекта. Это - программа сочетания химиотерапии с присоединением 2 таргетных препаратов (Трастузумаб+Пертузумаб), так называемая "двойная блокада".
Выбранный протокол лечения обладает относительно низкой токсичностью, что позволило пациентке после каждого курса лечения лететь домой в Ростовскую область и возвращаться к работе и активной жизни.
Начальный клинический эффект от выбранного режима был достигнут уже после первого введения препаратов, что проявилось значительным уменьшением опухолевого образования молочной железы более чем на 50% и уменьшением региональных лимфоузлов. Благодаря подобранной сопроводительной терапии (противорвотные, кардиопротекторы, гепатопротекторы), мы провели все 6 курсов химиотаргетной терапии вовремя, без задержек и переносов, с хорошим самочувствием пациентки.
После завершения неоадъювантной химиотаргетной терапии, пациентке была выполнена радикальная операция. При микроскопическом исследовании операционного материала был выявлен полный гистологический патоморфоз опухоли, наивысшая степень ответа на лечение - опухолевых клеток в материале обнаружено не было.
После успешно проведенной операции пациентка ушла на динамическое наблюдение, и теперь будет прилетать в нашу клинику раз в 3 месяца.
Выбранная программа сочетания химиотерапии и таргетной терапии с последующей операцией дает пациентке максимально высокие шансы на длительный период без рецидива болезни. Если вспомнить, что до начала терапии у пациентки была запущенная стадия болезни и агрессивный подтип опухоли, в прежние времена (до появления таргетной терапии) шансы получить такой беспрецедентный результат были равно 0, и болезнь неуклонно и быстро прогрессировала бы, несмотря на химиотерапию.
Полученный нами ответ на новую программу лечения является выдающимся результатом и значительным достижением клинической онкологии.
В сентябре 2015 года в нашу клинику пришел мужчина на заочную консультацию. Его маме 1945 года рождения, проживающей на Украине, диагностировали аденокарциному левого легкого сT4N1M0.
По месту жительства ей была назначена стандартная химиотерапия. После проведения первого курса у пациентки резко ухудшилось самочувствие, развилась сильная слабость.
Прямо на консультации мы организовали сеанс связи через Скайп, чтобы задать уточняющие вопросы по самочувствию самой пациентке и назначить ей схему восстановления – что она сможет сделать самостоятельно, находясь на Украине.
Я назначил молекулярно-генетическое исследование, чтобы составить молекулярный портрет опухоли и определить возможность применения других видов лечения, в том числе таргетной терапии.
В полученных результатах исследования была обнаружена мутация EGFR в опухоли, что позволило мне назначить таргетную терапию. Одним из ключевых преимуществ таргетных препаратов данного класса является то, что они выпускаются в таблетированной форме и обладают минимальными побочными эффектами. Таким образом, мы можем курировать пациентку дистанционно.
Уже третий год пациентка продолжает принимать таргетные препараты, а ее сын приходит к нам на консультацию 1 раз в 3 месяца с результатами обследований, которые каждый раз показывают все большие улучшения.
Это подтверждает, что возможности клинической онкологии сегодня в сочетании с подбором правильной комбинации препаратов позволяют контролировать опухоль, продлевая жизнь пациентов на годы.
Лечащий врач – Базылев Андрей Сергеевич.
Сегодня мы хотим рассказать про такой побочный эффект таргетной терапии как кожная токсичность, и как с ним можно справиться.
В нашу клинику за помощью обратилась женщина 1951 г.р. с диагнозом "рак толстой кишки Т3N0M0". Она была радикально прооперирована в 2017 году, но в марте 2021 года возник рецидив - появились метастазы в яичниках с инвазией в левый мочеточник и по брюшине с канцероматозом.
Ей выполнили операцию, по результатам молекулярно-генетического исследования мутации KRAS и NRAS не были обнаружены. После операции в городском учреждении ей начали проводить адъювантную химиотаргетную терапию по схеме FolFOX+моноклональное антитело (анти-EGFR) с июля 2021 по февраль 2022 года.
Оба анти-EGFR препарата - и цетуксимаб, и панитумумаб - имеют общее побочное действие: кожную токсичность.
Уже после 2-го курса у пациентки начались характерные кожные осложнения в виде пустулезной сыпи на лице и спине. Известно, что чем сильнее выражена кожная токсичность, тем выше эффект от лечения, поэтому терапию продолжали.
Однако пациентке не давали должных рекомендаций по уходу за высыпаними, и она мучилась вплоть до 8 курса.
На 9 и 10 курсе химиотерапии по настоянию пациентки таргетный препарат отменили, т.к. степень токсичности доставляла огромный дискомфорт и страдания больной. Кожные высыпания нарастали: отек мягких тканей лица с прикрытием век, массивные гнойничковые элементы, слившиеся в сплошную корку по всему лицу - все это сопровождалось неимоверным зудом, жжением и болезненностью.
В таком состоянии она обратилась к нам за помощью в феврале 2022 года.
Мы незамедлительно начали интенсивную симптоматическую терапию: антибиотики, антигистаминные препараты, снимающие кожный зуд, анальгетики, кортикостероиды во внутривенной и местной форме с 7 по 11 февраля.
За 5 дней все симптомы полностью купировались, и последние 2 курса химиотаргетной терапии пациентка получала в условиях нашей клиники.
Выполнив контрольные обследования и увидев стабилизацию, мы перевели ее на поддерживающую терапию капецитабином с 02.2022.
В течение 7 месяцев уже на 2 контрольных обследованиях у нее сохраняется стойкая стабилизация без тягостной кожной токсичности.
Вовремя проведенное корректирующее лечение кожный реакций и смена противоопухолевой терапии позволила сохранить качество жизни и стабилизацию заболевания.
Таргетная терапия при раке молочной железы:
- Блокаторы рецептора человеческого эпидермального фактора роста 2 (HER2) - Трастузумаб (Герцептин), Пертузумаб (Перьета), Трастузумаб Эмтанзин (Кадсила), Трастузумаб Дерукстекан (Энхерту).При HER2-положительном раке молочной железы на поверхности опухолевых клеток присутствует повышенное количество HER2 белка. Это определяется как «HER2-положительный статус».
Герцептин (Трастузумаб) блокирует Her2neu рецепторы, которые реагируют на воздействие факторов роста опухолевой клетки и не дают ему действовать на них.
Использование Герцептина позволило впервые за последние 30-40 лет существенно увеличить общую выживаемость больных метастатическим раком молочной железы. А при использовании в адъювантном режиме у больных раком молочной железы на ранних стадиях Трастузумаб позволил вдвое снизить риск развития рецидива заболевания. - PARP-ингибиторы - таргетные препараты нового класса. Ингибиторы PARP, включая препараты линпарза (олапариб) и талзенна (талазопариб), разрешены к применению в лечении распространенного HER2-отрицательного рака молочной железы у пациентов с мутацией BRCA1 или BRCA2. Одной из причин, которые влияют на резистентность опухолевых клеток к химиотерапии, является их способность восстанавливать повреждения ДНК, вызванные химиопрепаратами.
Механизм PARP-ингибиторов основан именно на подавлении способности к восстановлению этих повреждений. Блокируя активность PARP–белка, PARP-ингибиторы, в частности, Олапариб и Талазопариб, запускают так называемую «запрограммированную смерть клетки» (апоптоз) и значительно усиливают действие химиопрепаратов. И снова пациенты возвращаются к активной жизни, так как наступает устойчивая и длительная ремиссия заболевания. - Ингибиторы циклин-зависимых киназ (CDK4/6). Это - класс особых препаратов, применяемых в комбинации с гормонотерапией при распространенным или метастатическим раком молочной железы, имеющим положительный статус HR (рецепторов гормонов) и отрицательный статус HER2 (рецептора эпидермального фактора роста человека 2-го типа).
Это – новейшие таргетные препараты Рибоциклиб (Кискали, Рисарг), Палбоциклиб (Ибранса), Абемациклиб (Верзенио) в таблетированной форме. Они являются селективными ингибиторами циклин-зависимых киназ 4 и 6, (CDK4/6), которые помогают замедлить прогрессирование рака путем ингибирования двух белков.
Эти белки при чрезмерной активации могут вызвать ускоренный рост и деление опухолевых клеток. Специфичность к CDK4/6 с повышенной точностью может играть роль в прекращении неконтролируемого деления опухолевых клеток, вызывая остановку клеточного цикла, тем самым подавляя рост опухоли. Открытие данного механизма противоопухолевого действия, который принципиально отличается от гормоно- или химиотерапии, было удостоено Нобелевской премии в области медицины в 2001 году. - Блокаторы рецепторов к эстрогену и препятствующие присоединению эстрогена - Тамоксифен и Торемифен.
- Ингибиторы ароматазы (подавляет жизнедеятельность раковых клеток, нуждающихся в эстрогене как стимуляторе роста) - Летрозол, Анастрозол, Экземестан.
Видео о механизмах лечении современными таргетными препаратами рака молочной железы:
Таргетная терапия при раке легкого
Таргетная терапия является важнейшим методом в лечении распространенного немелкоклеточного рака легких, который составляет более 85% случаев. Создание таргетных препаратов для терапии рака легкого стало настоящим прорывом в современной онкологии.Для определения терапевтических возможностей лечения рака легких необходимо провести молекулярно-генетическое исследование на биомаркеры:
- При наличии драйверных мутаций назначается таргетная терапия:
1. При наличии мутации EGFR: Гефитиниб (Иресса), Эрлотиниб (Тарцева), Афатиниб (Гиотриф), Осимертиниб (Тагриссо);
2. При транслокации ALK/ROS: Кризотиниб, Алектиниб, Бригатиниб, Церитиниб, Лорлатиниб;
3. При мутации BRAF/MEK: Дабрафениб+Траметиниб;
4. С 2021 года ASCO (Американское общество клинической онкологии) впервые учитывает мутации MET, RET, NTRK. - При экспрессии PD-L1 решается вопрос о назначении иммунотерапии в первой линии лечения (анти-PD1 моноклональные антитела);
- При отсутствии и драйверных мутаций, и экспрессии PD-L1 выбор режима химиотерапии происходит в соответствии с гистологическим типом опухоли, состоянием пациента.
Таргетная терапия при колоректальном раке
Существует две категории таргетных препаратов: ингибиторы сигнальных путей (иматиниб, трастузумаб, цетуксимаб) и ингибиторы ангиогенеза (бевацизумаб, сунитиниб).Лучшую общую выживаемость и выживаемость без прогрессирования у пациентов с метастатическим колоректальным раком демонстрируют комбинированные схемы ингибиторов рецептора эпидермального фактора роста (EGFR) и сосудистого эндотелиального фактора роста (VEGF).
- Рамуцирумаб (Цирамза)— рекомбинантые антитела человека против VEGF-2;
- Афлиберцепт (Залтрап) — химерный протеин, состоящий из молекул экстрацеллюлярных доменов рецепторов VEGF человека, связанных с Fc-фрагментом иммуноглобулина G1.
- Бевацизумаб (Авастин) — рекомбинантные гуманизированные IgG-1 антитела против растворимого VEGF-А, которые с высокой аффинностью связываются с молекулой-мишенью и блокируют патологические молекулярные пути, предотвращая связывание VEGF-А с соответствующим рецептором.
Регорафениб (Стиварга) — мультикиназный ингибитор, блокирующий активность нескольких протеинкиназ рецепторов. Доказал свою эффективность после прогрессирования на стандартных схемах лечения колоректального рака.
Цетуксимаб (Эрбитукс) представляет собой химерные моноклональные антитела (мыши/человека);
Панитумумаб (Вектибикс) — полностью гуманизированные моноклональные антитела к рецепторам EGFR;
Вемурафениб (Зелбораф) в комбинации с химиопрепаратами, Дабрафениб (Тафинлар)+Траметиниб (Мекинист): мутация V600E в BRAF наблюдается приблизительно в 5—9% случаев колоректального рака и может быть заблокирована.
Таргетная терапия при раке яичников
Олапариб (PARP-ингибитор) одобрен в качестве поддерживающей терапии эпителиального рака яичников и маточных труб, а также первичного перитонеального рака у взрослых больных с клинически значимой герминальной или соматической мутацией гена BRCA, которые добились частичного или полного ответа на платиносодержащую терапию первой линии.Фермент поли(АДФ-рибоза)-полимераза (ПАРП) устраняет повреждения ДНК и в здоровых, и в злокачественных клетках. Ученые доказали, что лекарства, препятствующие действию фермента ПАРП, усложняют починку ДНК в раковых клетках с мутацией BRCA1 или BRCA2. Многие опухолевые клетки из-за этого погибают.
Cтоимость таргетной терапии
- Разработка и исследование новых лекарств: процесс разработки, клинических испытаний новых молекул для таргетной терапии и вывода ее на рынок занимает много лет и требует колоссальных инвестиций от фармпроизводителя.
- Технологические затраты: производственный цикл, используемый в таргетной терапии, может быть высокозатратным. Он включает в себя высокотехнологичное оборудование, специализированные методы производства и контроля качества.
- Малая целевая аудитория: поскольку таргетная терапия часто направлена на конкретные генетические мутации или биомаркеры рака, спрос на эти лекарства может быть ограниченным по сравнению с более широко применяемыми химиопрепаратами. Это приводит к более высоким ценам на единицу продукции для окупаемости вложенных фармкомпанией средств.
- Исследовательская деятельность и инновации: непрерывное динамичное развитие новых технологий и подходов в лечении рака требует постоянных инвестиций в исследования и разработку новых молекул и лекарств, из которых далеко не все выйдут на рынок.
- Эксклюзивные лицензии и патенты: компании, разрабатывающие и производящие таргетные препараты, могут владеть эксклюзивными правами на производство и продажу этих лекарств, что позволяет им устанавливать более высокие цены в первые годы, пока действует патент.
Запись на прием
Запишитесь на первичный прием сегодня, чтобы получить подробную консультацию и узнать, как таргетная терапия может помочь в вашей борьбе с раком. Ваше здоровье — наш главный приоритет.
Цены на услуги
- Консультация онколога 4 500
-
Внутривенное капельное введение противоопухолевых средств через Инфузомат Space
5 800
независимо от длительности введения
- Дистанционная консультация по телефону 5000
-
Пребывание в одноместной палате дневного стационара
4 200
повышенной комфортности, 1-я категория, с наблюдением среднего медицинского персонала
-
Круглосуточное пребывание в 1-местной палате стационара
8 900
включая 3-разовое питание
Отзывы
Узнать больше
Тверезовская Ирина Александровна
Подробнее











